La gestación tiene lugar desde la implantación del cigoto en el útero hasta el momento del parto. Desde el punto de vista metabólico, durante la gestación existen dos etapas bien diferenciadas: 1) en los dos primeros tercios, predomina una fase denominada anabólica, en la que la gestante aumenta su peso corporal debido a una lipogénesis activa que permite el acúmulo de tejido adiposo; y 2) en el último tercio, el metabolismo materno se invierte y entra en una fase denominada catabólica, en la que tiene lugar la movilización de la reservas maternas a través de la placenta para asegurar el correcto crecimiento del feto (1). Es importante destacar que durante estas dos fases existen variaciones en las hormonas gestacionales y placentarias, que tienen efecto en la concentración y la sensibilidad a la insulina para dar lugar a unos niveles de glucosa maternos adecuados. Esta glucosa será proporcionada al feto a través de la placenta durante la gestación para el adecuado embarazo a término. Por tanto, durante el embarazo, la madre presenta una mayor acumulación de tejido adiposo, además de presentar hiperinsulinemia y resistencia a la insulina.
Existen evidencias científicas que sugieren un papel importante de los receptores nucleares PPARγ, que regulan la sensibilidad a la insulina. Los receptores PPARγ tienen una función clave en el proceso de la adipogénesis o formación del tejido adiposo y en el almacenamiento de lípidos. También mejoran la sensibilidad a insulina periférica gracias a que disminuyen los ácidos grasos en la circulación e impiden que éstos se acumulen en otros tejidos. Durante el embarazo, el receptor PPARγ genera modificaciones a nivel de la célula-βeta pancreática, la célula del páncreas que produce insulina, aumentando no sólo en su tamaño sino también en número, para poder aumentar la secreción de insulina materna. También se produce un incremento de células que utilizan la glucosa y los lípidos circulantes en exceso, por lo que mejora la respuesta a la insulina durante la gestación. Otra función importante del receptor PPARγ durante la gestación es su participación en la diferenciación o maduración de los trofoblastos (células clave para la implantación del embrión al endometrio de la madre), así como en la detección de nutrientes en la placenta. Especialmente, este receptor aumenta la expresión de transportadores de ácidos grasos en la misma, favoreciendo el transporte materno-fetal. En definitiva, el receptor PPARγ juega un papel fisiológico esencial tanto en la sensibilidad a la insulina materna (a través del tejido adiposo y la célula-βeta pancreática), como en las funciones placentarias dirigidas al transporte de nutrientes desde la madre al feto. En la actualidad, uno de los problemas que se asocia frecuentemente con la gestación es el sobrepeso y la obesidad (2,3). En esta situación, se producen alteraciones en la expresión del receptor PPARγ en la célula-βeta pancreática y en el tejido adiposo. Estas alteraciones pueden generar complicaciones maternas con el desarrollo de diabetes gestacional (DMG), con repercusión en el desarrollo fetal y el metabolismo adulto de la descendencia.
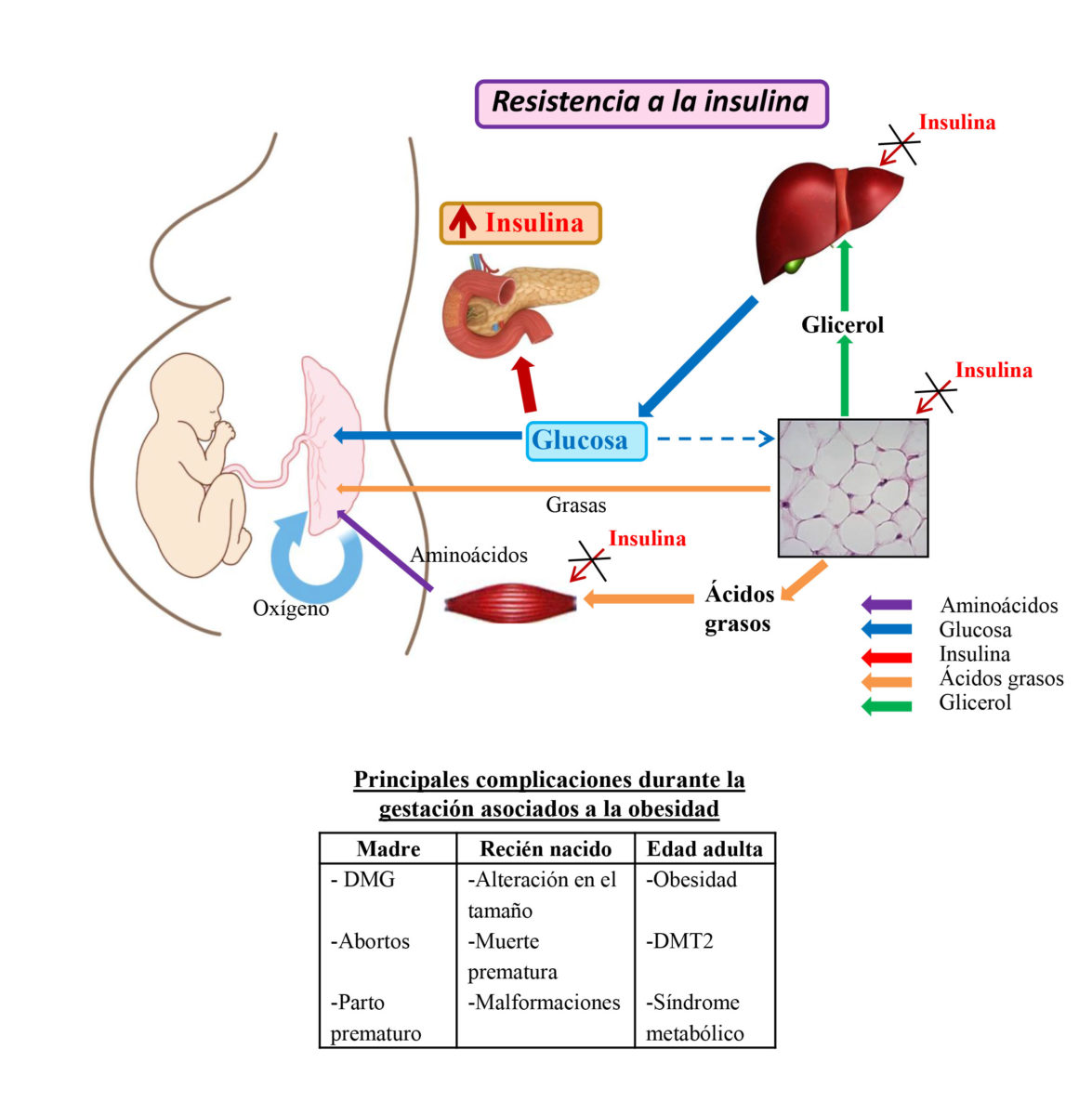
El embarazo es considerado un estado diabetogénico debido a la hiperinsulinemia (4). Comenzar un embarazo con sobrepeso u obesidad origina un aumento de la resistencia a insulina, lo que ocasiona un agotamiento de la capacidad de las células-βeta pancreáticas de secretar la cantidad de insulina requerida por el embarazo, dando lugar a un aumento de glucosa periférica (5). Ante esta situación, se produce una llegada masiva de nutrientes de la madre al feto, dando lugar a un aumento excesivo del tamaño fetal, así como a alteraciones metabólicas, cardiovasculares y malformaciones en el neonato e incluso llegar a su muerte prematura.
Otro problema durante la gestación con obesidad es que el propio tejido adiposo comienza a liberar una mayor cantidad de ácidos grasos a la circulación sanguínea por las posibles alteraciones en la expresión del receptor PPARγ que se mencionaban. Así, se acumula grasa en otros tejidos como el músculo y el hígado, entre otros, dando lugar al fenómeno tóxico conocido como lipotoxicidad. Además, conforme se expande el tejido adiposo, este tejido acumula cada vez más grasa y dispara mecanismos inflamatorios y de infiltración de células del sistema inmunitario denominadas macrófagos (6). Esta respuesta inflamatoria exagerada en el tejido adiposo y en la placenta conduce a un estado crónico de inflamación que puede originar incluso la disminución de la transferencia de oxígeno desde la madre al feto a través de la placenta.
Por ello, un control de peso antes del embarazo y el correcto diagnóstico y tratamiento de la resistencia a insulina y de la DMG durante el embarazo es fundamental tanto para la madre como para el feto, y así evitar problemas metabólicos en edad adulta de esos recién nacidos (7).
REFERENCIAS
- Rodríguez VM; Simón E. Bases de la alimentación humana. Editorial Oleiros, La Coruña Netiblo, 2008. https://books.google.es/books/about/Bases_de_la_Alimentaci%C3%B3n_Humana.html?id=c_f5eJ77PnwC
- Protocolos asistenciales en Obstetricia. Obesidad y embarazo. www.prosego.com
- Ramos MP. Obesidad y diabetes en la gestación: ¿dos caras de la misma moneda? CEU Universidad San Pablo. Diciembre 2014. http://dspace.ceu.es/bitstream/10637/6688/1/LecciónMagistralFarmacia2014.pdf
- M. J. Cerqueira. El diagnóstico de la diabetes gestacional. Prog Obstet Ginecol 2001;44:8-16.
- Rojas-Rodriguez R, Lifshitz LM, Bellve KD, Min SY, Pires J, Leung K, et al. Human adipose tissue expansion in pregnancy is impaired in gestational diabetes mellitus. Diabetologia. 2015; 58(9): 2016-14.
- Vivas Y, Díez-Hochleitner M, Izquierdo- Lahuerta A, Corrales P, Horrillo D, Velasco I, Martínez-García C, Campbell M, Sevillano J, Ricote M, Ros M, Ramos MP, Medina-Gomez G. Peroxisome proliferator activated receptor gamma 2 modulates late pregnancy homeostatic metabolic adaptations. Mol Med. 2016 Oct 19;22.
- European Obesity Day: https://www.europeanobesityday.eu/